免疫治疗生物标志物——联合为王
【2019-10-15】
免疫治疗可谓是上个月刚刚过去的CSCO大会上火热的话题,每一场相关讲座都是人山人海。
随着免疫检查点抑制剂(ICI)在中国正式获批和临床应用的实际开展,我们对于有效生物标志物的需求也与日俱增。目前已获批的标志物如PD-L1、MMR、MSI等在不同癌种中的表现存在差异,作为单独的疗效预测指标仍有所不足。本次大会上各位专家也针对更有效的免疫治疗biomarker进行了深入而广泛的讨论。
随着对肿瘤免疫的认识加深,我们已经察觉到肿瘤对免疫的逃逸不仅仅涉及到PD-1/PD-L1通路,在新生抗原产生、呈递、识别、T细胞浸润、杀伤等过程中出现问题都有可能导致肿瘤细胞从免疫系统的攻击中幸存,这些关键步骤涉及到的biomarker也在不断涌现。尽管各位专家提到的marker不尽相同,但总的共识和趋势是追求多marker联合检测以提升预测的准确性。
那么,到底有哪些marker获得了专家们的认可,有潜力成为免疫治疗预测标志物“联盟”中的一员呢?快来和大阅哥一起看看吧!
01 新抗原生成——TMB
肿瘤突变负荷(Tumor Mutation Burden, TMB)一般指肿瘤基因组每百万碱基所含有的非同义体细胞突变的数量,是反映肿瘤细胞携带的突变总数的一种定量生物标志物。如图1所示,MSKCC的Timothy A. Chan研究组最早于2014年发现,恶性黑色素瘤患者中,接受CTLA-4抗体治疗效果好的患者往往具有较高的肿瘤体细胞突变[1]。于2015年,他们最早提出了TMB的概念,并指出TMB的高低与非小细胞肺癌(NSCLC)患者使用PD-1抗体药物的疗效、预后显著相关[2]。Checkmate-026的回顾性研究报道了TMB高表达的NSCLC患者中使用抗PD-1药物的疗效显著优于对照组的铂类化疗药物。相比于化疗,使用免疫检查点抑制剂Nivolumab的中位PFS为9.7月v.s. 5.8月 (HR=0.62);客观缓解率从28.3%提高到46.8%[3]。这引发了临床研究对于TMB的兴趣,也使得TMB成为肺癌领域冉冉升起的具有潜力的新兴标志物,从而写入NCCN指南。目前一般认为TMB高导致了更多的新生抗原产生,使得肿瘤细胞更容易被免疫系统识别,因此在使用ICI激活免疫杀伤作用后疗效更好。
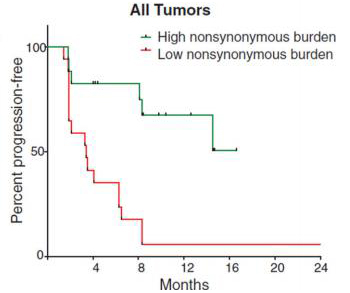
图1 Chan等发现突变数量高的NSCLC患者具有更好的免疫治疗疗效
然而,TMB在临床实践中遇到了不少问题。例如各家机构对于TMB的定义、算法都有所争议。目前各机构普遍采用NGS大panel来检测TMB,以降低测序成本。尽管各家的研究显示WES和panel测序所得TMB结果具有良好一致性,然而如图2所示,一项多机构进行的TMB一致性研究显示不同实验室panel-TMB和WES-TMB的一致性变异较大,Spearman's 系数为0.56~0.97,提示了TMB指标标准化的挑战[4];NGS测序仍具有一定的技术、成本问题,尚难以在临床中被广泛应用;此外,TMB的预测能力也受到了新研究的挑战。KEYNOTE-021[5]和KEYNOTE-189[6]研究都显示,TMB无法作为免疫治疗联合化疗的标志物。专家表示这可能是因为化疗会杀伤肿瘤细胞并释放肿瘤相关抗原,增强了ICI的疗效,从而影响到了TMB与疗效的相关性。
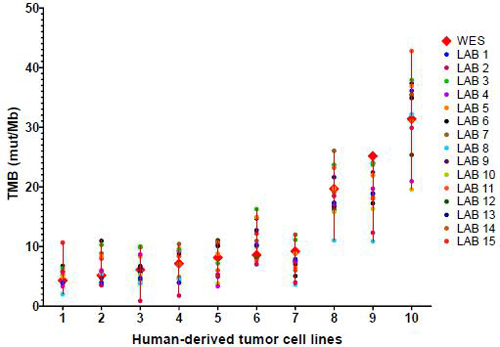
图2 TMB一致性研究结果
注:不同机构实验室对同一细胞系的测序结果存在差异,且随着TMB值的增高,不同实验室间差异增大。
02 抗原呈递——HLA-I
HLA-I类分子分布于几乎所有有核细胞表面,负责将内源性抗原呈递至细胞表面。研究发现一些患者的肿瘤细胞缺失HLA-I分子,使得CD8+ T细胞无法识别肿瘤细胞,从而造成肿瘤的免疫逃逸。
Chowell等人的研究表明,HLA-I分子的基因型与患者使用ICI的疗效显著相关[8]。若患者的HLA-I相关的三个基因位点全部为杂合型,则其疗效显著优于有至少一个位点为纯和型的患者。此外,生存分析表明HLA-I发生胚系杂合型缺失的患者,其生存显著变差。对于发生HLA-I杂合缺失且具有较低突变负荷的患者,其生存显著低于发生HLA-I杂合缺失但具有较高突变负荷的患者。这与我们的理论解释是相符的,疗效/生存最差的患者是那些即没有很多新生抗原,又难以将抗原呈递至细胞表面引发免疫反应的患者。
早期细胞系研究表明,B2M基因突变是导致黑色素瘤细胞系HLA-I缺失的重要原因之一[7]。而近年来的临床回顾性研究也发现了使用ICI后疾病进展的肺癌[9]及黑色素瘤[10]患者体内出现B2M突变及HLA-I缺失。B2M基因参与了HLA-I分子的折叠及细胞膜转运。当B2M基因失活,HLA-I分子无法正确地表达在癌细胞表面,使得CD8+ T细胞失去识别该肿瘤细胞的能力。
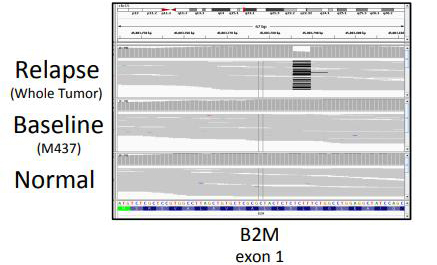
图3 黑色素瘤患者使用ICI进展后出现HLA-I缺失
注:测序结果表明,肿瘤复发后样本的B2M基因的Exon1发生了移码缺失突变,可能为HLA-I缺失的原因[10]。
03 T细胞浸润——肿瘤微环境
肿瘤所处微环境与正常的体内环境不同,往往具有缺氧、pH值偏低、存在M2型肿瘤相关巨噬细胞Treg细胞等特点,是一种免疫抑制的环境。处于此环境中的CD8+T细胞(肿瘤浸润淋巴细胞, TIL)的数量和状态显然与免疫治疗的疗效密切相关。
在KEYNOTE-028研究的次要终点中对T细胞炎症基因表达谱和ICI疗效的关系[11]进行了研究。KEYNOTE-028是一项篮子实验,其次要终点分析中纳入313名患者,涉及20个癌种。这些患者PD-L1表达阳性,且都接受了ICI治疗。研究者从患者治疗前的石蜡组织切片中提取RNA,分析了共18个T细胞炎症基因的表达水平,并据此计算不同患者的T细胞炎症基因表达谱得分。此得分可以整体性地评估各个患者地肿瘤微环境中T细胞的状态。结果显示,评分和患者疗效相关,评分更高的患者亚组拥有更高的ORR及更长的PFS。
一些肿瘤的微环境中存在TGFβ上调。TGFβ可以促进Treg细胞产生,并抑制CD8+ T细胞、DC细胞等免疫细胞的产生和功能,具有免疫抑制的功能。小鼠模型研究都表明,肿瘤微环境中的TGFβ抑制了ICI的疗效。通过阻断TGFβ信号通路,可以回复肿瘤细胞对ICI治疗的响应[12];而一项使用阿特珠单抗治疗尿路上皮细胞癌的临床实验结果显示,阿特珠单抗治疗无效与患者肿瘤相关成纤维细胞分泌的TGFβ显著相关[13]。提示我们TGFβ通过抑制效应T细胞浸润及抗肿瘤炎症反应造成了肿瘤的免疫逃逸。另有两项研究在临床前和I期临床实验中表明,同时针对TGFβ和PD-L1的双功能抗体具有良好的治疗效果[14, 15]。
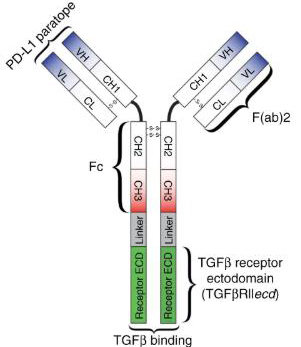
图4 双功能抗体
注:其轻链端可以结合PD-L1,而重链端则连接着TGFβ受体[14]。
篇幅所限,大阅哥这里也只是介绍了众多潜在标志物中的一部分,其它biomarker,例如STK11突变、PTEN缺失、β-catenin通路激活、IFNγ通路异常/JAK突变、肿瘤体细胞拷贝数变异、肠道微生物等等,都在不同层面的研究中显示了一定的预测或预后能力,在大会的不同讲座中获得了专家们的关注。
标志物如此之多,到底哪些是有效,且可用于实践中的,还需要更多的研究、尤其是更多前瞻性研究来证明,可以说道路还是艰苦而漫长的。Dr. Carbone教授风趣地评论道:“第一篇描述EGFR的论文发表在1962年,24年后作者获得了诺贝尔奖,再经过17年后IPASS研究证明了EGFR突变是EGFR-TKI的标志物;PD-1阻滞剂和免疫疗法的第一篇论文发表于1992年,26年后的2018年作者获得了诺贝尔奖。这样算来,希望我们能在2035年前看到ICI准确biomarker的出现。”
尽管前路漫漫,但我们已经走在了正确的路上;尽管各位专家提到的生物标志物有所差异,但总的共识已经出现。考虑到肿瘤免疫涉及步骤多、过程复杂,我们很可能需要一套组合的marker来评估患者的肿瘤免疫状态,以实现肿瘤免疫治疗的准确诊断、准确分组、准确治疗。在攻克肿瘤的道路上,我们一起前行。
阅微基因也在这条路上努力做出自己的贡献。阅微基因MSI检测试剂盒早在2011年就获得了国家专利,且与多家顶级临床机构进行了验。至今已检测数万例样本,积累了丰富的中国人群MSI临床数据库。通过准确检测患者MSI状态,我们为ICI组合marker贡献了一份力量。如果您有兴趣了解更多,欢迎随时和我们联系。
参考文献
1. Snyder, Alexandra, et al. Genetic basis for clinical response to CTLA-4 blockade in melanoma. New England Journal of Medicine 371.23 (2014): 2189-2199.
DOI: 10.1056/NEJMoa1406498
2. Rizvi, Naiyer A., et al. Mutational landscape determines sensitivity to PD-1 blockade in non–small cell lung cancer. Science 348.6230 (2015): 124-128.
DOI: 10.1126/science.aaa1348
3. Peters, Solange, et al. Abstract CT082: Impact of tumor mutation burden on the efficacy of first-line nivolumab in stage iv or recurrent non-small cell lung cancer: An exploratory analysis of CheckMate 026. AACR Annual Meeting 2017: CT082-CT082.
DOI: 10.1158/1538-7445.AM2017-CT082
4. Merino D, McShane L, et al. TMB standardization by alignment to reference standards: Phase II of the Friends of Cancer Research TMB Harmonization Project. 2019 ASCO. Board #2624.
DOI: 10.1200/JCO.2019.37.15_suppl.2624
5. Langer C, Gadgeel S, et al. KEYNOTE-021: TMB and Outcomes for Carboplatin and Pemetrexed With or Without Pembrolizumab for Nonsquamous NSCLC. WCLC 2019, OA04.05.
6. Garassino M, Rodriguez-Abreu D, et al. Evaluation of TMB in KEYNOTE-189: Pembrolizumab Plus Chemotherapy vs Placebo Plus Chemotherapy for Nonsquamous vs NSCLC. WCLC 2019, OA04.06.
7. d'Urso, C. M., et al. Lack of HLA class I antigen expression by cultured melanoma cells FO-1 due to a defect in B2m gene expression. The Journal of clinical investigation 87.1 (1991): 284-292.
DOI: 10.1172/JCI114984
8. Chowell, Diego, et al. Patient HLA class I genotype influences cancer response to checkpoint blockade immunotherapy. Science 359.6375 (2018): 582-587.
DOI: 10.1126/science.aao4572
9. Gettinger, Scott, et al. Impaired HLA class I antigen processing and presentation as a mechanism of acquired resistance to immune checkpoint inhibitors in lung cancer. Cancer discovery 7.12 (2017): 1420-1435.
DOI: 10.1158/2159-8290
10. Zaretsky, Jesse M., et al. Mutations associated with acquired resistance to PD-1 blockade in melanoma. New England Journal of Medicine 375.9 (2016): 819-829.
DOI: 10.1056/NEJMoa1604958
11. Ott, Patrick A., et al. T-cell–inflamed gene-expression profile, programmed death ligand 1 expression, and tumor mutational burden predict efficacy in patients treated with pembrolizumab across 20 cancers: KEYNOTE-028. Journal of Clinical Oncology 37.4 (2019): 318-327.
DOI: 10.1200/JCO.2018.78.2276
12. Tauriello D., Palomo-Ponce S., et al. TGFβ drives immune evasion in genetically reconstituted colon cancer metastasis. Nature 2018, 544: 538-543.
DOI: 10.1038/nature25492
13. Mariathasan S., Turley S., et al. TGFβ attenuates tumour response to PD-L1 blockade by contributing to exclusion of T cells. Nature 2018, 554: 544-548.
DOI: 10.1038/nature25501
14. Ravi R, Noonan K, et al. Bifunctional immune checkpoint-targeted antibody-ligand traps that simultaneously disable TGF-β enhance the efficacy of cancer immunotherapy[J]. Nature communications, 2018, 9(1): 741.
DOI: 10.1038/s41467-017-02696-6
15. Strauss J, Heery C, et al. Phase 1 trial of M7824 (MSB0011359C), a bifunctional fusion protein targeting PD-L1 and TGF-β, in advanced solid tumors[J]. Clinical Cancer Research, 2018: clincanres. 2653.2017.
DOI: 10.1158/1078-0432.CCR-17-2653







