从最新FIGO分期看子宫内膜癌分子分型临床应用
近期大家期待已久的2023年子宫内膜癌FIGO分期已经发布,推荐对所有子宫内膜癌进行完整的分子分型(POLEmut、MMRd、NSMP,p53abn),如果已知分子亚型,在FIGO分期中添加代表分子分类的字母“m”和下标分子亚型,当分期为I期和II期的肿瘤,分子分型为p53abn或POLEmut时,会导致肿瘤分期的上调或下调(IICmp53abn或IAmPOLEmut)[1]。

新的FIGO分期对于子宫内膜癌的分型更加细致,便于对子宫内膜癌患者更好的进行预后风险分层,并对辅助或全身治疗决策提供重要的参考依据。鉴于子宫内膜癌分子分型越来越重要的地位,下面我们一起梳理分子分型在子宫内膜癌诊疗过程中的临床应用。
1983年Bokhman依据临床病理学特征和预后将子宫内膜癌分为Ⅰ型和Ⅱ型两种类型[2]。由于Bokhman分型过于简单,Ⅰ型和Ⅱ型定义标准相对模糊,重现性不好;且对患者复发风险分层不够精确,在指导后续治疗选择上的作用非常有限,无法有效指导临床实践,临床急需重复性更好,对治疗指导更有意义的分类方法[3]。

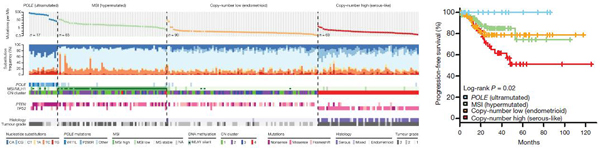
2013年,癌症基因组图谱(The Cancer Genome Atlas,TCGA)研究利用多组学分析提出子宫内膜癌分子分型,依据分子表型判断预后,分为4个亚型:POLE 超突变型(ultramutated)、MSI高突变型 (hypermutated)、Copy-number low (endometrioid)和Copy-number high (serous-like),其中POLE超突变型发生率约7%,预后最好;Copy-number high型发生率约为26%,预后最差;而MSI-H型和Copy-number low 型发生率分别28%和39%,预后中等[4]。
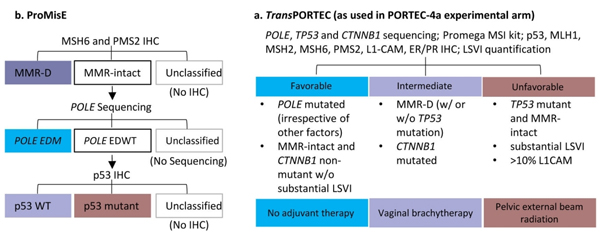
2015年,Talhouk等提出ProMisE分型方法,采用错配修复蛋白(MMR)、p53免疫组化和POLE基因突变检测,将子宫内膜癌分为4个亚型,该分型与TCGA分型高度一致[5]。而2016年,Stelloo等在ProMisE分型的基础上,结合L1CAM高表达(>10%)、CTNNB1外显子3突变和淋巴血管间隙浸润,进一步提出Trans-PORTEC分型,对中高危患者进行精准的风险分层[6]。
随着分子分型临床实践不断深入,子宫内膜癌NCCN指南、ESGO指南、CSCO指南中推荐对所有确诊子宫内膜癌患者进行分子分型检测,用于风险评估和治疗指导。另外最新的《卵巢子宫内膜样癌临床诊治中国专家共识(2023年版)》中建议对卵巢子宫内膜样癌推荐有条件时进行分子检测和分子分型,其中POLE超突变型约5%,错配修复蛋白缺陷型约13%,TP53突变型约9%-13%和无特异性分子改变型约69%-73%[7]。
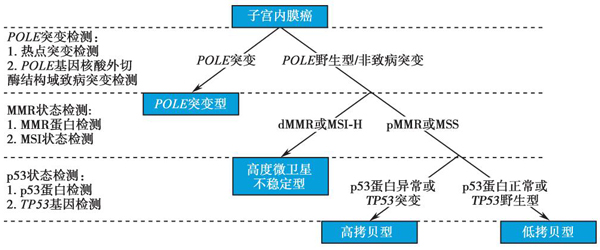
子宫内膜癌分子分型判读流程 来源:2023 CSCO子宫内膜癌诊疗指南
辅助病理分型:TCGA的研究数据显示,同一病理类型中存在不同的基因变异,临床预后差异大。另外分子分型在不同病理类型中的比例不同,在所有子宫内膜癌病例中POLEmut型占6%-8%,而在高级别子宫内膜癌样癌中高达15%[8]。据统计病理学家将约25%的肿瘤归类为高级别子宫内膜样癌,但其分子表型类似于子宫浆液性癌。2020年第五版WHO女性生殖器官肿瘤分类将子宫内膜癌分子分型纳入标准病理报告中。
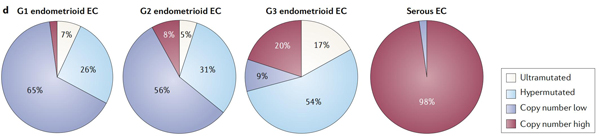
预后指导:根据TCGA子宫内膜癌分子分型研究,POLE超突变型预后最好,高拷贝数型预后最差,MSI高突变型和低拷贝数型预后中等。最近来自小样本研究中强调MSI高突变型肿瘤中可能存在多样性,与LS相关的MSI-H子宫内膜癌患者相比,MLH1缺失患者的预后更差,对免疫治疗的反应更低[9],由于样本量比较少,期待更大规模样本研究数据来验证在分子亚型中进行生物标志物分层的必要性。2021年ESGO/ESTRO/ESP联合发布将分子分型纳入风险组分配,并为每个风险组提供直接辅助治疗建议。其中I-II期,无残留病灶、POLEmut型子宫内膜癌为低危组,无需额外治疗[10]。2023 FIGO分期指出将分子分型纳入到分期标准中可以更好的指导预后预测。
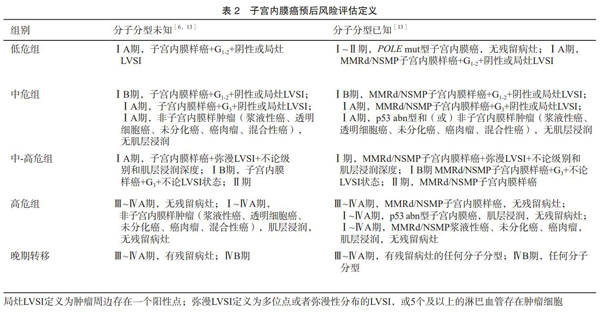
*对于III-IVA期POLEmut子宫内膜癌和I-IVA期MMRd或NSMP透明细胞癌伴有肌层浸润,没有足够的数据将这些患者在分子分类中分配到预后风险组。
辅助治疗指导:分子分型对辅助治疗具有指导作用,《子宫内膜癌诊断与治疗指南》中指出POLE超突变型预后极好,这类患者如果手术分期为I-II期,术后可考虑随访,不做辅助治疗[11],POLE超突变肿瘤被认为对免疫检查点抑制剂(ICI)免疫治疗的潜在获益者[12]。MMRd/MSI-H型对免疫治疗敏感,基于KEYNOTE-158研究,FDA已批准pembrolizumab用于不可手术或转移的dMMR/MSI-H实体瘤的后线治疗。PORTEC-3研究评估辅助放化疗对高危子宫内膜癌的5年生存率影响,结果显示,与辅助放疗相比,辅助放化疗能显著改善p53abn患者的PFS,而对于POLE mut患者,无统计学差异[13]。NSMP患者对激素治疗敏感,年轻患者保育治疗效果较好。
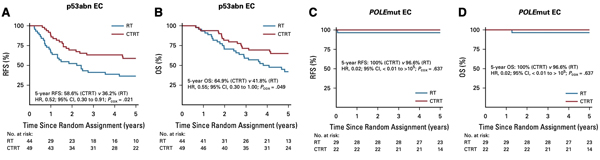
林奇综合征筛查:子宫内膜癌中林奇综合征的发生率约为3%-5%,《2023 CSCO 子宫内膜癌诊疗指南》推荐对所有新确诊的子宫内膜癌患者进行MMR/MSI状态检测,用于林奇综合征筛查[14]。

来源:2023 CSCO子宫内膜癌诊疗指南
子宫内膜癌分子分型的特征总结:不同分子分型子宫内膜癌的临床特征、预后、组织病理学特点、分子特征以及治疗表现是不同的,根据现有指南利用分子分型进行回顾性研究发现,33%的POLEmut EC患者接受了过度治疗,而42%的p53abn ECs患者可能治疗不足[15],提示我们需要充分利用分子分型来更好的指导子宫内膜癌预后风险分层及辅助治疗。
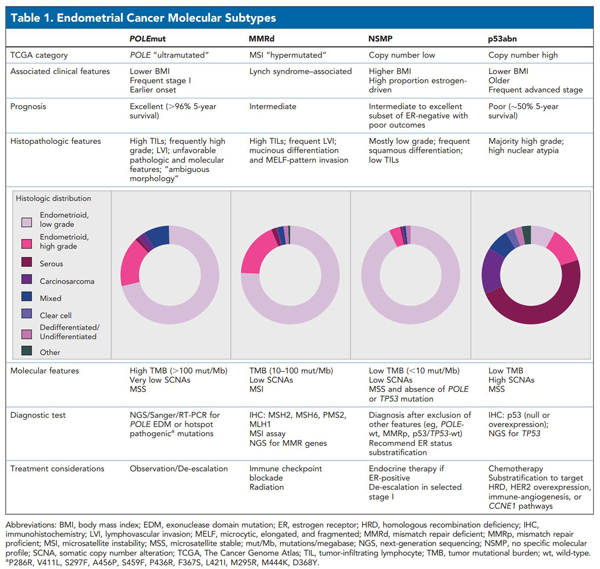
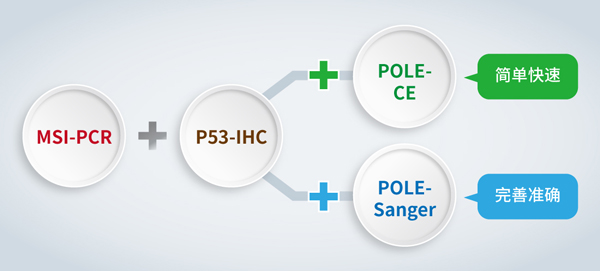
为了分子分型更好的运用到子宫内膜癌的临床应用中,分子分型的检测至关重要,《子宫内膜癌分子检测中国专家共识(2021年版)》优先建议POLE基因热点突变检测(Sanger测序)、MMR蛋白检测(免疫组织化学法)/MSI检测(PCR法)和p53蛋白检测(免疫组织化学法)进行分子分型。
阅微基因率先推出两款基于一代测序平台的POLE基因突变检测产品:POLE基因突变检测试剂盒(荧光PCR-毛细管电泳法)和POLE基因突变检测试剂盒(qPCR-Sanger测序法),简称POLE-CE法和POLE-Sanger法,其中POLE-CE法可在一个反应体系中同时检测已知公认11个热点突变位点,简单快速;POLE-Sanger法可检测9-14号外显子上所有突变,完善准确;搭配阅微基因已获批的微卫星不稳定基因检测试剂盒(国械注准20213400936)以及p53蛋白免疫组化,从两个维度满足不同客户需求,助力子宫内膜癌分子分型整体解决方案。